อัตราการเกิดปฏิกิริยาเคมี
作者:uthaiwan rortsuwan
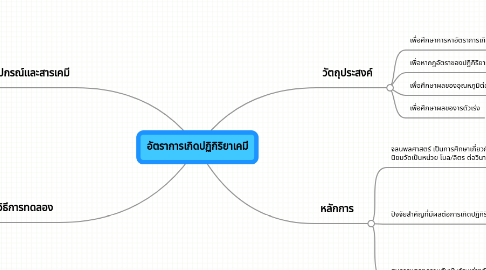

1. อุปกรณ์และสารเคมี
1.1. โพแทสเซียมไอโอไดด์ 0.200M
1.2. แอมโมเนียมเปอร์ซัลเฟต 0.100M
1.3. โพแทสเซียมคลอไรด์ 0.200M
1.4. แอมโมเนียมซัลเฟต 0.100 M
1.5. โซเดียมไทโอซัลเฟต 0.005 M
1.6. น้ำแป้ง 1%
1.7. คอปเปอร์(||) ซัลเพฃฟต 0.1 M
1.8. ปิเปตขนาด 10 ลบ.ซม.
1.9. ขวดรูปชมพู่
1.10. เทอร์โมมิเตอร์
1.11. นาฬิกาจับเวลา
2. วิธีการทดลอง
2.1. ตอนที่1 ผลของความเข้มข้น ต่ออัตราการเกิดปฏิกิริยา และการหากฎอัตรา
2.2. ตอนที่2 ผลของอุณหภูมิต่ออัตราการเกิดปฏิกิริยา และหาค่าพลังงานกระตุ้นของปฏิกิริยา
2.3. ตอนที่3 ผลของตัวเร่ง
3. วัตถุประสงค์
3.1. เพื่อศึกษาการหาอัตราการเกิดปฏิกิริยาเคมี
3.2. เพื่อหากฎอัตราของปฏิกิริยาระหว่างไอออนเปอร์ออกซิไดซัลเฟตและไอออนไอโอไดด์
3.3. เพื่อศึกษาผลของอุณหภูมิต่ออัตราการเกิดปฏิกิริยาและหาค่าพลังงงานกระตุ้นของปฏิกิริยา
3.4. เพื่อศึกษาผลของารตัวเร่ง
4. หลักการ
4.1. จลนพลศาสตร์ เป็นการศึกษาเกี่ยวกับอัตราการเกิดปฏิกิริยา และกลไกลการเกิดปฏิกิริยา อัตราการเกิดปฏิกิริยาวัดได้จากการเปลี่ยนแปลงความเข้มข้นของสารต่อหน่วยเวลา นิยมวัดเป็นหน่วย โมล/ลิตร ต่อวินาที
4.2. ปัจจัยสำคัญที่มีผลต่อการเกิดปฏิกิริยา
4.2.1. ธรรมชาติของสารตั้งต้น
4.2.2. ความเข้มข้นของสารตั้งต้น
4.2.3. อุณหภูมิ
4.2.4. ตัวเร่ง
4.3. สมการแสดงความสัมพันธ์ระหว่างอัตราการเกิดปฏิกิริยากับความเข้มข้นของสารตั้งต้น
4.3.1. Rate= ค่าคงที่คูณด้วยผลคูณของความเข้มข้นของสารตั้งต้นยกกำลังด้วยอันดับของปฏิกิริยา
