KEMI
af Pernilla Brunkwall
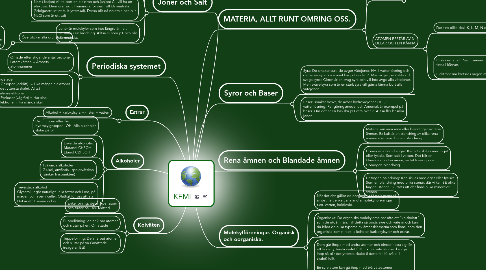

1. Joner och Salt
1.1. En possetiv jon bildas när en atom ger bort en elektron.
1.2. En nagativ jon bildas när en atom tar emot en elektron
1.3. Na+ ( katjon) vill ta bort en elektron och (anjon) Cl- vlil ha en elektron. Dem drar sig till varandra för dem vill bli neutrala (ädelgasstruktur= fullt ytterskal). Dessa blir då neutrala och blir NaCl som är ett salt
1.4. Joner är molekyler som inte längre är helt neutrala i sin laddning. Alltså e- som p+ och blir då neutrala.
2. Periodiska systemet
2.1. Överblickar alla grundämnen.
2.1.1. Delas in i: ° Metaller ° Halvmetaller ° Ickemetaller
2.2. Ornade efter stigande antal protoner i atomkärnan = Ämnets atomnummer
2.3. Indelade i ° Grupper (lodrätt). = Lika många elektroner i det yttersta skalet. Alltså valenselektroner. °Perioder (vågrätt) = Har sina elektroner i lika många skal
3. Alkoholer
3.1. Det finns en eller fler hydroxylgrupper - OH. Alla alkoholer slutar på ol
3.2. Envärda alkoholer: Metanol CH3OH Etanol C2H5OH
3.3. Tvåvärda alkoholer: Glukol, används i spolarvätskan (sänker fryspunkten)
3.4. Trevärdiga alkohol Glycerol, ingår naturligt i alla fetter och i oss, på magen och även i celler. Ofatligt för oss att äta. Det är ett E ämne också
4. Estrar
4.1. Alkohol + karbxylsyra --> ster + vatten
5. Kolväten
5.1. Enkel bining: delar 1 par atom och slutar på - an. Mättad
5.2. Bubbelbining: delar 2 par atomer och slutar på en. Omättade
5.3. Trippelbining: Delar 3 pat atomer och slutar på yn Omättade (reagerar lätt)
6. MATERIA, ALLT RUNT OMRING OSS.
6.1. DEMOKRITOR-ALL MATERIA KUNDE DELAS I MINDRE BITAR
6.2. Protoner +1 Neutoner 0 Elektroner-1
6.2.1. I varje Proton finns 3 kvark
6.3. ATOMEN BESTÅR AV 3 DELAR OCH EN KÄRNA
6.3.1. Det fins olika skal. K, L, M, N ovs.
6.3.1.1. K= 2 elektroner
6.3.1.2. L= 8 elektroner
6.3.1.3. M= 18elektroner
6.3.1.4. N= 32 elektroner
6.3.2. Protonerna och Neutronenerna finna i kärnan. Elektronerna kretsar i någon av salen

