1. Ácidos
1.1. Íons H+ em água
1.1.1. Formando Hidroxônio
1.2. Sofrem ionização
1.2.1. Em etapas: 1 íon por vez
1.3. Classificação
1.3.1. Quanto aos compostos
1.3.1.1. Hidrácidos
1.3.1.1.1. Sem Oxigênio
1.3.1.2. Oxiácidos
1.3.1.2.1. Com Oxigênio
1.3.2. Quanto aos H ionizáveis
1.3.2.1. Monopróticos Dipróticos Tripróticos Tetrapróticos
1.3.2.2. Nos Hidrácidos: todos são Nos Oxiácidos: apenas os ligados ao O
1.3.3. Quanto Volatilidade
1.3.3.1. Voláteis (ou gases)
1.3.3.2. Fixos (ou sólidos)
1.3.4. Quanto à força
1.3.4.1. Oxiácidos: O-H
1.3.4.1.1. 3: muito forte 2: forte 1: moderados 0: fraco <0: muito fraco
1.3.4.2. Hidrácidos
1.3.4.2.1. Fortes: HCl, HBr, HI Moderados: HF Fracos: Demais
1.3.4.3. Orgânicos
1.3.4.3.1. Sempre fracos
1.3.4.4. Grau de ionização
1.3.4.4.1. >50%: Forte 5%-50%: Moderado <5%: Fraco
1.4. Nomenclatura
1.4.1. Hidrácidos: Ácido + Ânion - Eto + Ídrico
1.4.2. Oxiácidos:
1.4.2.1. Ácido + Ânion - Ito + Oso
1.4.2.2. Ácido + Ânion - Ato + Ico
1.4.2.3. +1 O: Per ... Ico -1 O: ...Oso -2 O: Hipo ... Oso
1.4.3. mosquITO - teimOSO te mATO - te pICO te mETO - no vÍDRICO
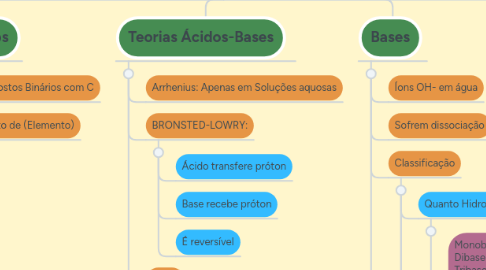
2. Bases
2.1. Íons OH- em água
2.2. Sofrem dissociação
2.3. Classificação
2.3.1. Quanto Hidroxilas
2.3.1.1. Monobase Dibase Tribase Polibase
2.3.2. Quanto à força
2.3.2.1. Forte: Alcalinos Terrosos Fraca: Demais metais
2.3.3. Quanto à solubilidade
2.3.3.1. Solúveis: Amônia e Metais Alcalinos Parcial: Alcalinos Terrosos (Mg e Be não) Insolúveis: Demais
2.4. Nomenclatura
2.4.1. Hidróxido de (Metal)
2.4.1.1. Oso para o menor Nox Ico para o maior Nox
3. Sais
3.1. Vem da reação de neutralização
3.2. Classificação
3.2.1. Neutro: H+ = OH- Hidrogenossais: H+ > OH- Hidroxissais: H+ < OH-
3.3. Nomenclatura
3.3.1. Neutros: Ânion de Cátion
3.3.2. Ácidos: Prefixo + Hidrógeno + Ânion de Cátion
3.3.3. Básicos: Prefixo + Hidroxi + Ânion de Cátion
3.3.4. Duplos: Prefixo + Ânion de Prefixo + Cátion
3.3.5. Hidratados: Ânion de Cátion + Prefixo + Hidratado
3.4. Propriedades
3.4.1. Sólidos cristalinos
3.4.2. Alto PF e PE
3.4.3. Conduzem corrente elétrica em água ou quando fundidos
3.4.4. Solúveis em Solventes Polares
3.4.5. Sofrem dissociação em água
4. Óxidos
4.1. Compostos Binários Mais eletronegativo: Oxigênio
4.2. Óxidos Iônicos (Básicos)
4.2.1. Oxigênio com Nox = -2
4.2.2. Metais Alcalinos, A.Terrosos ou de Transição com Nox > 6
4.2.3. de Metais Alcalinos e A.Terrosos em água formam bases
4.2.4. reagem com ácidos formando sal e água
4.2.5. Nomenclatura
4.2.5.1. Óxido de (Metal)
4.3. Óxidos Moleculares (Ácidos ou Anidridos)
4.3.1. Oxigênio com Nox = -2
4.3.2. Não metais ou Metais com Nox > 4
4.3.3. Reagem em água formando ácido
4.3.4. Reagem com bases formando sal e água
4.3.5. Nomenclatura
4.3.5.1. Prefixo + Óxido de Prefixo + Elemento
4.4. Óx. Ácido + Óx Básico = SAL
4.5. Óxidos Antóferos
4.5.1. Principais: BeO, ZnO, Al2O3, MnO2, SnO, SnO2, PbO, PbO2, As2O3, As2O5, Sb2O3 e Sb2O5.
4.5.2. Ora comportam-se como ácido Ora comportam-se como básico
4.5.3. Reagem apenas com ácidos e bases FORTES
4.6. Óxidos Neutros
4.6.1. Não reagem
4.6.2. Formados por ametais
4.6.3. Moleculares e Gasoso
4.7. Óxidos Duplos (misto)
4.7.1. dois óxidos do mesmo elemento
4.7.2. Fórmula geral: M3O4
4.7.2.1. Fe3O4 (Fe2O3 ∙ FeO): TETRÓXIDO DE TRIFERRO
4.7.3. Reagem com ácido ou base, formando dois sais e água
4.8. Peróxido
4.8.1. H, Alcalinos e A.Terrosos
4.8.2. De fórmula geral M2O2 ou MO2
4.8.3. Nomenclatura
4.8.3.1. Peróxido de (Elemento)
4.8.4. Oxigênio como Ânion -2 Nox = -1
4.8.5. H2O2: PERÓXIDO DE HIDROGÊNIO Na2O2: PERÓXIDO DE SÓDIO MgO2: PERÓXIDO DE MAGNÉSIO
4.9. Superóxido
4.9.1. Oxigênio como Ânion -1 Nox = -0,5
4.9.2. Alcalinos e A.Terrosos
4.9.3. Reagem com água, produzindo bases, H2O2 e O2
4.9.4. NaO2: SUPERÓXIDO DE SÓDIO Mg(O2)2: SUPEÓXIDO DE MAGNÉSIO KO2: SUPERÓXIDO DE POTÁSSIO Ca(O2)2: SUPERÓXIDO DE CÁLCIO
5. Hidretos
5.1. Compostos Binários com H
5.2. Metálicos
5.2.1. H com Nox = -1
5.2.2. Hidreto de (Metal)
5.3. Não Metálicos
5.3.1. H com Nox = +1
5.3.2. Água, Metano, Amônia...
6. Carbetos
6.1. Compostos Binários com C
6.2. Carbeto de (Elemento)
7. Teorias Ácidos-Bases
7.1. Arrhenius: Apenas em Soluções aquosas
7.2. BRONSTED-LOWRY:
7.2.1. Ácido transfere próton
7.2.2. Base recebe próton
7.2.3. É reversível
7.3. Lewis
7.3.1. Ácidos recebem parer de elétrons
7.3.2. Bases doam pares de elétrons
7.3.3. formação de ligação covalente coordenada mais estável
