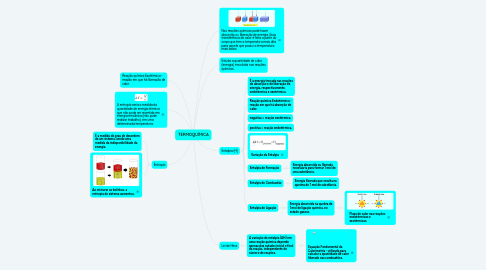
TERMOQUÍMICA
por Bruna Beal

1. Reação química Exotérmica - reação em que há liberação de calor.
2. A entropia seria a medida da quantidade de energia térmica que não pode ser revertida em energia mecânica (não pode realizar trabalho), em uma determinada temperatura.
3. Entropia
3.1. É a medida do grau de desordem de um sistema, sendo uma medida da indisponibilidade da energia.
3.2. Ao misturar as bolinhas, a entropia do sistema aumentou.
4. Nas reações químicas pode haver absorção ou liberação de energia. Essa transferência de calor é feita a partir do corpo que tem a temperatura mais alta para aquele que possui a temperatura mais baixa.
5. Estuda a quantidade de calor (energia) envolvida nas reações químicas.
6. Entalpia (H)
6.1. É a energia trocada nas reações de absorção e de liberação de energia, respectivamente, endotérmica e exotérmica.
6.2. Reação química Endotérmica - reação em que há absorção de calor.
6.3. negativa = reação exotérmica.
6.4. positiva = reação endotérmica.
6.5. Variação da Entalpia
6.6. Entalpia de Formação
6.6.1. Energia absorvida ou liberada necessária para formar 1 mol de uma substância.
6.7. Entalpia de Combustão
6.7.1. Energia liberada que resulta na queima de 1 mol de substância.
6.8. Entalpia de Ligação
6.8.1. Energia absorvida na quebra de 1 mol de ligação química, no estado gasoso.
6.8.1.1. Fluxo de calor nas reações endotérmicas e exotérmicas.
7. Lei de Hess
7.1. A variação de entalpia (ΔH) em uma reação química depende apenas dos estados inicial e final da reação, independente do número de reações.
7.1.1. Equação Fundamental da Calorimetria - utilizada para calcular a quantidade de calor liberado nas combustões.
