ÁCIDOS Y BASES
von Jiménez Mendez Hannia
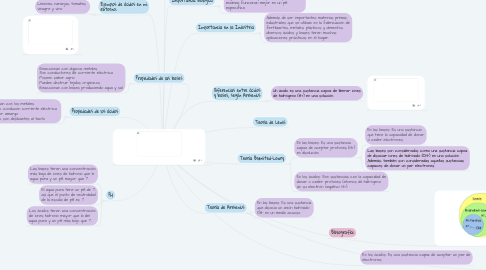

1. Propiedades de las bases
1.1. Reaccionan con algunos metales. Son conductores de corriente eléctrica. Poseen sabor agrio Pueden destruir tejidos orgánicos. Reaccionan con bases produciendo agua y sal.
2. Propiedades de los ácidos
2.1. No reaccionan con los metales. En disolución, conducen corriente eléctrica. Poseen sabor amargo En disolución, son deslizantes al tacto
3. Ejemplos de ácidos en mi entorno:
3.1. Limones, naranjas, tomates, vinagre y vino.
4. Ejemplos de bases en mi entorno:
4.1. Leche de magnesia, pasta dental, jabón (u otros detergentes) y bicarbonato de sodio.
5. PH
5.1. Las bases tienen una concentración más baja de iones de hidronio que le agua pura y un pH mayor que 7.
5.2. El agua pura tiene un pH de 7, así que el punto de neutralidad de la escala de pH es 7.
5.3. Los ácidos tienen una concentración de iones hidronio mayor que la del agua pura y un pH más bajo que 7.
6. Ácidos y bases: reacciones químicas y aplicaciones
7. Ácidos, Bases y Sales
8. ¿Qué propiedades físicas presentan los ácidos y las bases?
9. En los ácidos: Es una sustancia capaz de aceptar un par de electrones.
10. En los ácidos: Es una sustancia que libera iones de hidrógeno H+ en solución acuosa.
11. Teorías de ácidos-bases: Arrhenius, Bronsted-Lowry, Lewis
12. 22/03/2021
13. Tema: Características e importancia, biológica, ecológica y económica de los ácidos y bases
14. Importancia biológica
14.1. Los ácidos y bases son importantes en los organismos vivos porque la mayoría de las enzimas funcionan mejor en un pH específico.
15. Diferencias entre ácidos y bases, según Arrhenius
15.1. Un ácido es una sustancia capaz de liberar iones de hidrógeno (H+) en una solución.
16. Teoría de Lewis
17. Teoría Brønsted-Lowry
17.1. En las bases: Es una sustancia capaz de aceptar protones (H+) en disolución.
17.1.1. En las bases: Es una sustancia que tiene la capacidad de donar o ceder electrones.
17.1.2. Las bases son consideradas como una sustancia capaz de disociar iones de hidróxido (OH-) en una solución. Además, también son consideradas aquellas sustancias capaces de donar un par electrones.
