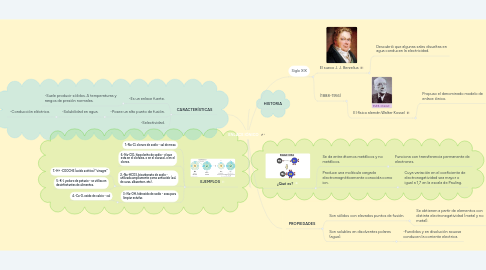
1. CARACTERÍSTICAS
1.1. -Es un enlace fuerte.
1.1.1. -Suele producir sólidos. A temperaturas y rangos de presión normales.
1.2. -Posee un alto punto de fusión.
1.2.1. -Solubilidad en agua.
1.2.1.1. -Conducción eléctrica.
1.3. -Selectividad.
2. EJEMPLOS
2.1. 1.-Na-Cl, cloruro de sodio - sal de mesa
2.2. 6.-Na-ClO, hipoclorito de sodio - el que esta en el cloralex, o en el clarasol, o en el clorox.
2.3. 2.-Na-HCO3, bicarbonato de sodio - utilizada ampliamente como antiacido (sal, de uvas, alkasetser, etc).
2.3.1. 7.-H+ -COOCH3 (acido acético) “vinagre”
2.3.2. 5.-K-I, yoduro de potasio - se utiliza en desinfectantes de alimentos.
2.4. 3.-Na-OH, hidroxido de sodio - sosa para limpiar estufas
2.4.1. 4.-Ca-O, oxido de calcio - cal
3. Siglo XIX
3.1. El sueco J. J. Berzelius
3.1.1. Descubrió que algunas sales disueltas en agua conducen la electricidad.
3.2. (1888-1956)
3.2.1. El físico alemán Walter Kossel
3.2.1.1. Propuso el denominado modelo de enlace iónico.
4. HISTORIA
5. ¿Qué es?
5.1. Se da entre átomos metálicos y no metálicos.
5.1.1. Funciona con transferencia permanente de electrones.
5.2. Produce una molécula cargada electromagnéticamente conocida como ion.
5.2.1. Cuya variación en el coeficiente de electronegatividad sea mayor o igual a 1,7 en la escala de Pauling.
6. PROPIEDADES
6.1. Son sólidos con elevados puntos de fusión.
6.1.1. Se obtienen a partir de elementos con distinta electronegatividad (metal y no metal).
6.2. Son solubles en disolventes polares (agua).
6.2.1. -Fundidos y en disolución acuosa conducen la corriente electrica.

