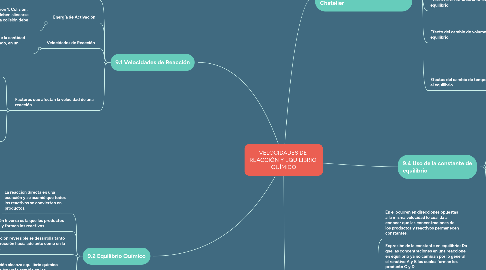
1. 9.2 Equilibrio Químico
1.1. La reacción directa en una ecuación y se asumió que todos los reactivos se convierten en productos.
1.2. La reacción Inversa es la que los productos se reúnen y forman los reactivos.
1.3. La reacción reversible se desarrolla tanto en la dirección hacia adelante como en la inversa.
1.3.1. Es decir que hay dos velocidades de reacción: la velocidad de reacción recta y la inversa.
1.4. Una reacción alcanza equilibrio químico cuando no hay más cambio en las concentraciones de los reactivos o productos, incluso cuando las dos reacciones continúan a velocidades iguales pero opuestas.
1.4.1. En el equilibrio:
1.4.1.1. *La velocidad de la reacción directa es igual a la velocidad de la reacción inversa.
1.4.1.2. *No ocurren más cambios en las concentraciones de los reactivos o productos; las reacciones directa e inversa continúan a velocidades iguales.
1.5. Reacción Directa
1.5.1. H2 (g) + I2 (g) -> 2HI (g)
1.6. Reacción Inversa
1.6.1. H2 (g) + I2 (g) <- 2HI (g)
2. 9.1 Velocidades de Reacción
2.1. La teoría de colisiones indica que una reacción tiene lugar sólo cuando las moléculas chocan con la orientación adecuada y con suficiente energía.
2.1.1. Debe haber suficiente energía para romper los enlaces entre los átomos de los reactivos. La energía de activación es la cantidad mínima de energía necesaria para romper los enlaces entre los átomos de los reactivos
2.2. Energía de Activación
2.2.1. Tres condiciones indispensables para que ocurra una reacción 1. Colisión: Los reactivos deben chocar. 2. Orientación: Los reactivos deben alinearse correctamente para romper y formar enlaces. 3. Energía: La colisión debe suministrar la energía de activación.
2.3. Velocidades de Reacción
2.3.1. Para determinar la velocidad (o rapidez) de reacción se mide la cantidad de un reactivo agotado, o la cantidad de un producto formado, en un lapso determinado.
2.4. Factores que afectan la velocidad de una reacción
2.4.1. Temperatura:
2.4.1.1. A temperaturas más altas, el aumento de energía cinética hace que las moléculas que reaccionan se muevan más rápido, ocurren más colisiones, y más moléculas que chocan tienen suficiente energía para reaccionar y formar productos.
2.4.2. Concentraciones de los Reactivos:
2.4.2.1. Virtualmente en todas las reacciones, la velocidad de una reacción aumenta cuando las concentraciones de los reactivos aumentan. Cuando hay más moléculas en reacción pueden ocurrir más colisiones que formen productos y la reacción avanza más rápido.
2.4.3. Catalizadores:
2.4.3.1. Otra forma de acelerar una reacción es reducir la energía de activación. Un catalizador acelera una reacción al reducir la energía de activación, lo que permite que más colisiones de los reactivos tengan suficiente energía para formar productos.
3. 9.5 Cambio en las condiciones de equilibrio: el principio de Le Chatelier
3.1. El pirncipio de Le Chatelier
3.1.1. Cuando un sistema en equilibrio se perturba, el sistema se desplazará en la dirección que reduzca dicha pertubación.
3.2. Efectos de los cambios de concentración sobre el equilibrio
3.2.1. H2 + I 2= 2HI
3.2.1.1. Agregar H2
3.2.1.1.1. El sistema se desplaza en dirección a los reactivos.
3.2.1.1.2. Se desencadena una pertubación y aumenta su velocidad.
3.2.1.2. Eliminar H2
3.2.1.2.1. El sistema se desplazará en dirección de los reactivos.
3.2.1.2.2. Velocidad de la reaccion directa frena.
3.2.1.3. Agregar HI
3.2.1.3.1. El sistema se desplazará en dirección de los reactivos.
3.2.1.3.2. Aumento en la velocidad de la reacción en dirección inversa.
3.2.1.4. Eliminar HI
3.2.1.4.1. El sitema se desplazará en dirección a los productos.
3.3. Efecto de un catabilizador sobre el equilibrio
3.3.1. Acelera las reacciones directa e inversa, son provocar algún cambio en las concentraciones de los reactivos y productos.
3.4. Efecto del cambio de volumen sobre el equilibrio
3.4.1. Reducir el volumen
3.4.1.1. Aumenta la concentración de gases.
3.4.1.2. El sistema se debe desplazar en la dirección del menor número de moles.
3.4.2. Aumentar el volumen
3.4.2.1. Disminuye la concentración de los gases,
3.4.2.2. El sistema se dezplazará en dirección al mayor número de moles.
3.5. Efectos del cambio de temperatura sobre el equilibrio
3.5.1. Reacción Endotérmica
3.5.1.1. Amento de temperatura
3.5.1.1.1. Se desplazara en dirección de los productos.
3.5.1.2. Disminuye la temperatura
3.5.1.2.1. Se desplazará en dirección de los reactivos.
3.5.2. Reacción Exotérmica
3.5.2.1. Aumenta la temperatura
3.5.2.1.1. Se desplazará en dirección de los reactivos.
3.5.2.2. Disminuye la temperatura
3.5.2.2.1. Se desplazara en dirección de los productos.
