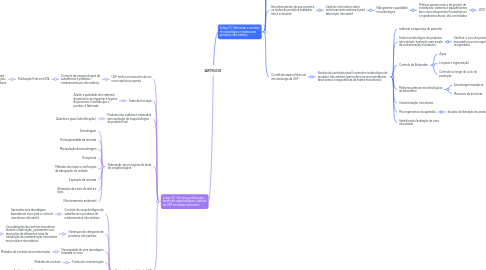
1. Artigo 01: Refinando o controle microbiológico e testes para produtos não estéreis
1.1. Produtos farmacêuticos deve ser seguro para o paciente
1.1.1. Microrganismos podem ter impacto adverso afetando as propriedades físico-químicas e o valor rerapêutico
1.1.2. Ausência de microrganismos potencialmente causadores de doenças
1.1.2.1. microrganismos censuráveis
1.2. Produtos não estéreis representam desafios
1.2.1. Não podem conter muitos microrganismos e qualquer microrganismo potencialmente nocivo
1.2.1.1. Não pode ser assegurado pelo teste do produto acabado
1.2.1.1.1. Limitações estatísticas de amostragem e ensaios microiológicos
1.3. Capítulos da USP: ênfase dada aos testes de materiais acabados
1.3.1. Menos atenção aos meios necessários para proteger os produtos
1.4. Reconhecimento de que somente os testes de produtos acabados não é suficiente
1.4.1. Capítulo informativo sobre monitoramento ambiental para fabricação não estéril
1.4.1.1. Não garante a qualidade microbiológica
1.4.1.1.1. Práticas operacionais e de projeto de instalações, sistemas e equipamentos, bem como excipientes farmacêuticos e ingredientes ativos, são controlados
1.5. Comitê de especialistas em microbiologia da USP
1.5.1. Revisão do conteúdo atual (controle microbiológico de produtos não estéreis) para refinar as recomendações de processo e expectativas de testes microbianos
1.5.1.1. melhorar a segurança do paciente
1.5.1.2. Teste microbiológico de produtos não estéreis: avaliação mais ampla da contaminação microbiana
1.5.1.2.1. Verificar o risco do paciente associado aos microrganismos recuperados
1.5.1.3. Controle de Bioburden
1.5.1.3.1. Água
1.5.1.3.2. Limpeza e higienização
1.5.1.3.3. Controle ao longo do ciclo de produção
1.5.1.4. Melhores práticas microbiológicas de laboratório
1.5.1.4.1. Amostragem asséptica
1.5.1.4.2. Manuseio de amostras
1.5.1.5. Caracterização microbiana
1.5.1.6. Microrganismos recuperados
1.5.1.6.1. decisão de liberação do produto
1.5.1.7. Identificação/avaliação de risco microbiano
2. Artigo 02: Um novo padrão para testes de carga biológica: capítulo da USP em desenvolvimento
2.1. USP emitiu um rascunho de um novo capítulo proposto
2.1.1. Controle de carga biológica de substâncias e produtos medicamentosos não estéreis
2.1.1.1. Publicação final em 2014
2.1.1.1.1. Estabelecimento de uma abordagem baseada no risco para monitorar e controlar as intalações e processos de fábrica de produtos farmacêuticos não estéreis
2.2. Teste de biocarga
2.2.1. Avaliar a qualidade dos materiais de partida e acompanhar a higiene do processo à medida que o produto é fabricado
2.3. Produtos não estéreis é necessária uma avaliação da carga biológica do produto final
2.3.1. Quantos e quais (identificação)
2.4. Elaboração de um regime de teste de carga biológica
2.4.1. Amostragem
2.4.2. Homogeneidade da amostra
2.4.3. Manipulação da amostragem
2.4.4. Recipiente
2.4.5. Métodos de ensaio e verificação da adequação do método
2.4.6. Expiração da amostra
2.4.7. Atribuição de níveis de alerta e ação
2.4.8. Monitoramento ambiental
2.5. Proposta de capítulo da USP
2.5.1. Controle de carga biológica de substâncias e produtos de medicamentos não estéreis
2.5.1.1. Apresenta uma abordagem baseada em risco para o controle microbiano não estéril
2.5.2. Hierarquia de categorias de produtos não estéreis
2.5.2.1. Considerações de controle microbiano durante a fabricação, juntamente com descrições de diferentes rotas de introdução de contaminação microbiana em produtos não estéries
2.5.2.1.1. Hierarquia de risco para o doente
2.5.3. Necessidade de uma abordagem baseada no risco
2.5.3.1. Métodos de controle da contaminação
2.5.4. Fontes de contaminação
2.5.4.1. Medidas de controle
2.5.5. Ingredientes farmacêuticos
2.5.5.1. Auditorias de fornecedores, especificações, testes, seleção de pacotes, envio, condições de armazenamento e datas de validade
2.5.6. Monitoramento ambiental
2.5.6.1. Informações sobre a seleção dos locais de amostragem e sobre a definição da frequência
2.5.7. Final do processo
2.5.7.1. Armazenamento dos produtos
2.5.7.1.1. Evitar a contaminação microbiana
2.5.8. Gerenciamento do programa de controle microbiológico para a fabricação de produtos não estéreis
2.5.8.1. Análise dos riscos, compreensão do produto, dos materiais, das instalações e da população de doentes
