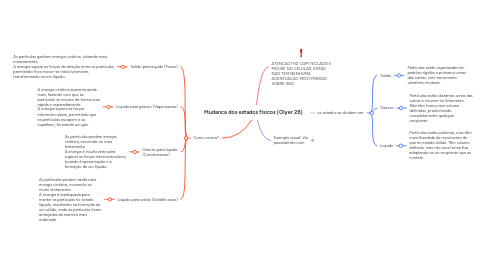
1. os estados se dividem em:
1.1. Solido
1.1.1. Partículas estão organizadas em padrões rígidos e próximos umas das outras, com movimento vibratório limitado.
1.2. Gasoso
1.2.1. Partículas estão distantes umas das outras e movem-se livremente. Não têm forma nem volume definidos, preenchendo completamente qualquer recipiente.
1.3. Liquido
1.3.1. Partículas estão próximas, mas têm mais liberdade de movimento do que no estado sólido. Têm volume definido, mas não uma forma fixa, adaptando-se ao recipiente que as contém.
2. Exemplo visual: Via passeidireto.com
3. ATENCAO! FIZ COM TECLADO E MOUSE NO CELULAR, ENTAO NAO TEM NENHUMA ACENTUACAO PECO PERDAO SOBRE ISSO
4. Como ocorre?
4.1. Solido para liquido (Fusao)
4.1.1. As partículas ganham energia cinética, vibrando mais intensamente. A energia supera as forças de atração entre as partículas, permitindo-lhes mover-se mais livremente, transformando-se em líquido.
4.2. Liquido para gasoso (Vaporizacao)
4.2.1. A energia cinética aumenta ainda mais, fazendo com que as partículas se movam de forma mais rápida e separadamente. A energia supera as forças intermoleculares, permitindo que as partículas escapem e se espalhem, formando um gás.
4.3. Gasoso para liquido (Condensacao)
4.3.1. As partículas perdem energia cinética, movendo-se mais lentamente. A energia é insuficiente para superar as forças intermoleculares, levando à aproximação e à formação de um líquido.
4.4. Liquido para solido (Solidificacao)
4.4.1. As partículas perdem ainda mais energia cinética, movendo-se muito lentamente. A energia é inadequada para manter as partículas no estado líquido, resultando na formação de um sólido, onde as partículas ficam arranjadas de maneira mais ordenada.
