rapidez das reações
por Pelzinhu Edits
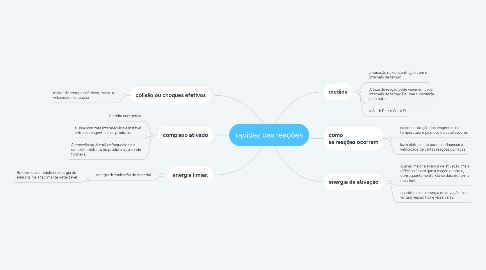
1. colisão ou choques efetivos
1.1. maior de choques efetivos, maior a velocidade da reação
2. complexo ativado
2.1. barreira energética
2.2. é uma estrutura intermediária e instável entre os reagentes e os produtos.
2.3. A conexão atual está enfraquecida e a conexão existente no produto está sendo formada.
3. energia limiar.
3.1. energia de ionização do material
3.1.1. Refere-se ao módulo de energia de elétrons mais facilmente detectável
4. medida
4.1. a variação da concentração com o intervalo de tempo
4.2. A taxa de reação pode variar em cada intervalo de tempo.De uma substância para outra.
4.3. a A + b B → c C + d D
5. como as reações ocorrem
5.1. na concentração dos reagentes, na temperatura e pelo uso de catalisadores
5.2. luz e eletricidade podem influenciar a velocidade de certas reações químicas
6. energia de ativação
6.1. quanto maior a energia de ativação, mais difícil será para que a reação ocorra e, consequentemente, ela se dará de forma mais lent
6.2. quanto maior a energia de ativação mais lenta a reação fica e visse versa.


