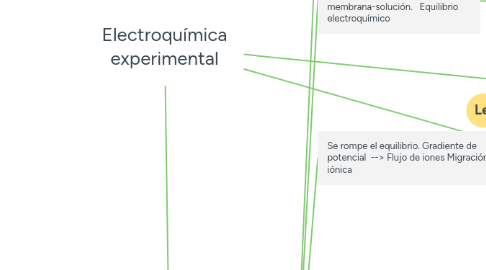
Electroquímica experimental
por Hernán Aristizábal

1. Etapa fenomenológica
1.1. Formación de disolución iónica Equilibrio químico
1.1.1. Condicionalidad química
1.2. Se forma la interfase polarizada; metal-solución; solución-solución; membrana-solución. Equilibrio electroquímico
1.2.1. NERNST-PETERS
1.2.1.1. POTENCIOMETRÍA-SENSORES Y BIOSENSORES
1.3. Se rompe el equilibrio. Gradiente de potencial --> Flujo de iones Migración iónica
1.3.1. KOHLRAUSCH
1.3.1.1. CONDUCTIMETRÍA- ELECTROFORESIS MIGRACIÓN ZONAL
1.4. Se rompe el capacitor de la interfase cargada: hay transferencia de carga a través de la interfase. Gradiente de concentración --> Difusión Reacción de transferencia Reacción electroquímica
1.4.1. COTTRELL
1.4.1.1. CRONOAMPEROMETRÍA
1.4.2. SAND
1.4.2.1. CRONOPOTENCIOMETRÍA
1.5. Se controla la cinética de los procesos interfaciales: A) Cinética electródica B) Cinética de transferencia de masa C) Cinética química acoplada
1.5.1. REGÍMENES NO ESTACIONARIOS SEVICK
1.5.1.1. VOLTEMPEROMETRÍ CÍCLICA - ULTRAMICROELECTRÓDOS
1.5.2. REGÍMENES ESTACIONARIOS LEVICH, ILKOVICK
1.5.2.1. VOLTAMPEROMETRÍA HIDRODINÁMICA - POLAROGRAFÍA CLÁSICA
1.5.3. METODOLOGÍAS ESPECIALES
1.5.3.1. COULOMBIMETRÍA STRIPPING ESPECTROELECTROQUIMCIA
