1. Clasificación por cambio de estructura
1.1. Reaccion de adicion
1.1.1. Como su nombre lo indica se adiciona una molécula al enlace para obtener compuestos olefinicos
1.2. Reaccion de eliminacion
1.2.1. Se basa en la perdida de atomos o un grupo dentro de la molecula
1.3. Reacción por sustitución
1.3.1. Grupo atómico reemplazado por otro
1.4. Reacción de oxido-reducción
1.4.1. Reacción química en donde se transfieren electrones entre los reactivos
1.4.1.1. Oxidacion
1.4.1.1.1. El agente reductor es aquel elemento químico que suministra electrones de su estructura química al medio, aumentando su estado de oxidación, es decir, siendo oxidado
1.4.1.2. Reduccion
1.4.1.2.1. El agente oxidante es aquel elemento químico que tiende a captar esos electrones, quedando con un estado de oxidación inferior al que tenía, es decir, siendo reducido
1.5. Reacción de transposición
1.5.1. Reestructuración de las moléculas para generar una estructura distinta
2. Clasificación
2.1. Reaccion de Homolisis
2.1.1. Cada fragmento, en la ruptura se lleva consigo electrones del enlace original según una ruptura simétrica.
2.2. Reaccion de heterolisis
2.2.1. Uno de dos fragmentos en el enlace se queda con dos electrones del enlace covalente original siguiendo una ruptura asimétrica.
2.3. Reaccion Perciclica
2.3.1. Una reacción pericíclica es una reacción concertada en la que el estado de transición tiene una geometría cíclica.
3. Sintesis de alcoholes
3.1. Los alcoholes se pueden obtener a partir de haloalcanos mediante reacciones SN2 y SN1
3.1.1. Sintesis de Alcoholes por reducción de carbonilos
3.1.1.1. Tanto el borohidruro de sodio (NaBH4) como el hidruro de litio y aluminio (LiAlH4) reducen aldehídos y cetonas a alcoholes.
3.1.2. Síntesis de Alcoholes por hidrogenación de Carbonilos
3.1.2.1. Otro método para preparar alcoholes consiste en la reducción de aldehídos o cetonas a alcoholes. El método más simple es la hidrogenación del doble enlace carbono-oxígeno, utilizando hidrógeno en presencia de un catalizador de platino, paladio, niquel o rutenio.
3.1.3. Sintesis de Alcoholes a partir de Epóxidos
3.1.3.1. Los alcoholes se pueden obtener por apertura de epóxidos (oxaciclopropanos). Esta apertura se puede realizar empleando reactivos organometálicos o el reductor de litio y aluminio.
3.1.4. Síntesis de Alcoholes por Hidratación de Alquenos
3.1.4.1. Un método de síntesis para alcoholes, ya estudiado en la sección de alquenos, consiste en hidratar el alqueno. La adición del -OH puede ser en el carbono más sustituido del alqueno (Markovnikov), o bien, en el carbono menos sustituido (antiMarkovnikov).
3.1.5. Síntesis de alcoholes por reducción de ácidos y ésteres
3.1.5.1. Los ácidos carboxílicos y los ésteres se reducen a alcoholes con el hidruro de litio y aluminio. Reductores más suaves como el borohidruro de sodio son incapaces de reducir estos compuestos.
3.1.6. Síntesis de Haloalcanos a partir de Alcoholes
3.1.6.1. Los alcoholes primarios y secundarios pueden convertirse en haloalcanos con reactivos como: tribromuro de fósforo, tricloruro de fósforo, cloruro de tionilo y pentacloruro de fósforo.
3.1.7. Oxidación de Alcoholes
3.1.7.1. La oxidación de alcoholes forma compuestos carbonilos. Al oxidar alcoholes primarios se obtienen aldehídos, mientras que la oxidación de alcoholes secundarios forma cetonas.
3.1.8. Formación de Alcóxidos a partir de Alcoholes
3.1.8.1. Los alcóxidos son las bases de los alcoholes, se obtienen por reacción del alcohol con una base fuerte.
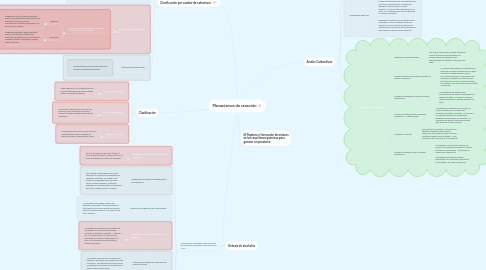
4. Ruptura y formación de enlaces en las reacciones químicas para generar un producto
5. Acidos Carboxilicos
5.1. Nomenclatura
5.1.1. La IUPAC nombra los ácidos carboxílicos reemplazando la terminación -ano del alcano con igual número de carbonos por -oico
5.2. Propiedades fisicas
5.2.1. Los ácidos carboxílicos son moléculas con geometría trigonal plana. Presentan hidrógeno ácido en el grupo hidroxilo y se comportan como bases sobre el oxígeno carbonílico.
5.3. Propiedades quimicas
5.3.1. Acidez:La propiedad más característica de los ácidos carboxílicos es la acidez del hidrógeno situado sobre el grupo hidroxilo. El pKa de este hidrógeno oscila entre 4 y 5 dependiendo de la longitud de la cadena carbonada.
5.3.2. Bacisidad:La protonación del grupo ácido se produce sobre el oxígeno del grupo carbonilo ya que la especie obtenida se estabiliza por resonancia, deslocalizando la carga positiva sobre el grupo hidroxilo.
5.4. Síntesis de Ácidos Carboxílicos
5.4.1. Oxidación de alquilbencenos
5.4.1.1. Los ácidos carboxílicos pueden obtenerse a partir de bencenos sustituidos con grupos alquilo por oxidación con permanganato de potasio o dicromato de sodio.
5.4.2. Síntesis de haluros de alcanoilo a partir de ácidos carboxílicos
5.4.2.1. Los haluros de alcanoilo se obtienen por reacción de ácidos carboxílicos con PBr3 . También se puede emplear SOCl2 . Así, el ácido etanoico se transforma en bromuro de etanoilo por reacción con tribromuro de fósforo. El ácido etanoico por reacción con cloruro de tionilo forma el compuesto.
5.4.3. Síntesis de Anhídridos a partir de Acidos Carboxílicos
5.4.3.1. Los hidrácidos se obtienen por condensación de ácidos carboxílicos con pérdida de agua. La reacción requiere fuerte calefacción y tiempo de reacción largo.
5.4.4. Síntesis de ésteres a partir de ácidos carboxílicos - Esterificación
5.4.4.1. Los ésteres se obtienen por reacción de ácidos carboxílicos y alcoholes en presencia de ácidos minerales. La reacción se realiza en exceso de alcohol para desplazar los equilibrios a la derecha. La presencia de agua es perjudicial puesto que hidroliza el éster formado.
5.4.5. Síntesis de Lactonas
5.4.5.1. Las lactonas son ésteres cíclicos que se obtienen mediante esterificación intramolecular a partir de moléculas que contienen grupos ácido y alcohol. Esta ciclación forma ciclos de 5 o 6 miembros.
5.4.6. Síntesis de amidas a partir de ácidos carboxílicos
5.4.6.1. Las amidas se forman por reacción de ácidos carboxílicos con amoniaco, aminas primarias y secundarias. La reacción se realiza bajo calefacción. A temperaturas bajas las aminas reaccionan con los ácidos carboxílicos como bases y no como nucleófilos.
