teorias ácidos-bases
por GRACILEIDE De JESUS OLIVEIRA
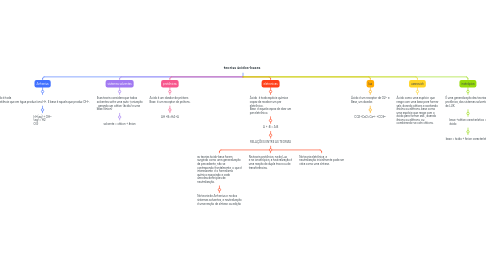

1. Arrhenius
1.1. ácido é toda substância que em água produz íons H+. E base é aquela que produz OH–.
1.1.1. H+(aq) + OH– (aq) = H2 O(l)
2. sistemas solventes
2.1. Essa teoria considera que todos solventes sofre uma auto -ionização , gerando um cátion (ácido) e uma base (ânion)
2.1.1. solvente = cátion + ânion
3. protônicas
3.1. Acido é um doador de prótons Base é um receptor de prótons.
3.1.1. AH +B=HA+A
4. eletronicas
4.1. Ácido é toda espécie química capaz de receber um par eletrônico. Base é aquela capaz de doar um par eletrônico.
4.1.1. A + :B = A:B
4.1.1.1. RELAÇÔES ENTRE AS TEORIAS
4.1.1.1.1. as teorias ácido-base foram surgindo como uma generalização da precedente, não se contrapondo frontalmente, o que é interessante é o formalismo químico associado a cada uma das definições de neutralização.
4.1.1.1.2. Na teoria protônica, na de Lux e na ionotrópica, a neutralização é uma reação de dupla troca ou de transferências.
4.1.1.1.3. Na teoria eletrônica, a neutralização inicialmente pode ser vista como uma síntese.
5. lux
5.1. Ácido é um receptor de O2– e Base, um doador.
5.1.1. CO2+CaO=Ca²+ +CO3²-
6. usanovich
6.1. Ácido como uma espécie que reage com uma base para formar saís, doando cátions e aceitando ânions ou elétrons .base como uma espécie que reage com o ácido para formar saís , doando ânions ou elétrons ,ou combinando-se com cátions.
7. inotrópica
7.1. É uma generalização das teorias protônica, dos sistemas solventes e de LUX.
7.1.1. base +cátion característico = ácido
7.1.1.1. base = ácido + ânion característico
