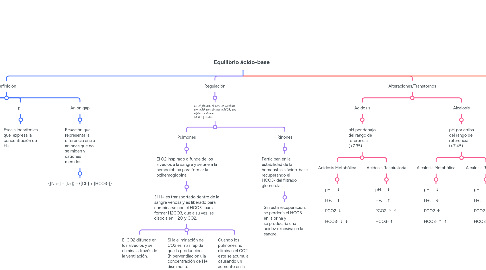
1. Definición
1.1. Ácido
1.1.1. Sustancia que puede ceder o donar H+ cuando se disuelve en agua.
1.2. Base
1.2.1. Sustancia que puede ceder OH- o aceptar H+
1.3. Disolución amortiguadora
1.3.1. Combinación de una base débil o ácido débil y su sal disociada o par conugado, es un sistema que resiste los cambios de pH.
1.4. pH
1.4.1. Escala logarítmica que expresa la concentración de H+
1.5. Anión gap
1.5.1. Ecuación que representa la diferencia entre aniones que no se miden y cationes medidos.
1.5.1.1. {[Na+] + [k+]} – {[Cl-] + [HCO3-]}
2. Regulación
2.1. En el plasma, el CO2 se combina con H2O para formar H2CO3, que rápido se disocia en H+ y HCO3-.
2.1.1. Pulmones
2.1.1.1. El O2 inspirado difunde de los alvéolos a la sangre y se une a la hemoglobina para formar la oxihemoglobina.
2.1.1.1.1. El H+ es transportado dentro de la sangre venosa y es liberado para combinarse con el HCO3- para formar H2CO3, que a su vez, se disocia en H2O y CO2.
2.1.2. Riñones
2.1.2.1. Participan en la estabilidad de la homeostasis ácido-base recuperando el HCO3- del filtrado glomerular.
2.1.2.1.1. Sin esta recuperación, se perdería el HCO3- en la orina y se produciría una acidez excesiva en la sangre.
3. Alteraciones/Transtornos
3.1. Acidosis
3.1.1. pH por debajo del rango de referencia (<7.35)
3.1.1.1. Acidosis Metabólica
3.1.1.1.1. pH. ↓ H+. ↑ PCO2. ↓ HCO3- ↓ ↓
3.1.1.2. Acidosis Respiratoria
3.1.1.2.1. pH. ↓ H+. ↑ PCO2. ↑ ↑ HCO3- ↑
3.2. Alcalosis
3.2.1. pH por arriba del rango de referencia (>7.45)
3.2.1.1. Alcalosis Metabólica
3.2.1.1.1. pH. ↓ H+. ↓ PCO2. ↑ HCO3- ↑ ↑
3.2.1.2. Alcalosis Respiratoria
3.2.1.2.1. pH. ↓ H+. ↓ PCO2. ↓ HCO3- ↓ ↓
4. Pruebas de laboratorio
4.1. Determinación espectrofotométrica de la saturación de oxígeno
4.1.1. Analizadores de gases en sangre: PH, PCO2 Y PO2
