1. Tinción de Gram
1.1. Procedimiento
1.1.1. 1. Preparar un frotis de la muestra y fijarlo con calor. 2.Aplicar cristal violeta durante 2-3 minutos. 3.Añadir lugol (mordiente) por 1 minuto. 4.Lavar con agua destilada. 5.Decolorar con alcohol al 96% 6.Aplicar safranina (colorante de 7.contraste) por 5 minutos. Lavar, secar y observar al microscopio
1.1.1.1. Identificación
1.1.1.1.1. preliminar de bacterias y orientación en el tratamiento antibiótico
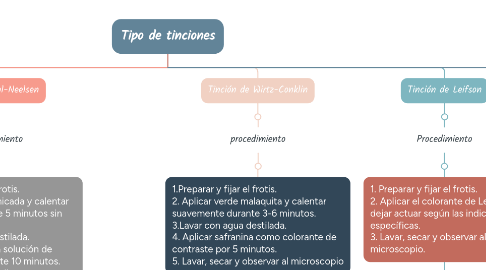
2. Tinción Ziehl-Neelsen
2.1. procedimiento
2.1.1. 1.Preparar y fijar el frotis. 2.Aplicar fucsina fenicada y calentar suavemente durante 5 minutos sin dejar hervir. 3.Lavar con agua destilada. 4.Decolorar con una solución de alcohol-ácido durante 10 minutos. 5.Aplicar azul de metileno como colorante de contraste por 3 minutos. 6.Lavar, secar y observar al microscopio.
2.1.1.1. Diagnostica
2.1.1.1.1. Diagnosticar tuberculosis y otras infecciones micobacterianas
3. Tinción de Wirtz-Conklin
3.1. procedimiento
3.1.1. 1.Preparar y fijar el frotis. 2. Aplicar verde malaquita y calentar suavemente durante 3-6 minutos. 3.Lavar con agua destilada. 4. Aplicar safranina como colorante de contraste por 5 minutos. 5. Lavar, secar y observar al microscopio
3.1.1.1. Identifica
3.1.1.1.1. bacterias formadoras de esporas, como Bacillus y Clostridium.
4. Tinción de Leifson
4.1. Procedimiento
4.1.1. 1. Preparar y fijar el frotis. 2. Aplicar el colorante de Leifson y dejar actuar según las indicaciones específicas. 3. Lavar, secar y observar al microscopio.
4.1.1.1. Estudia
4.1.1.1.1. Motilidad y clasificación de bacterias según la presencia y disposición de flagelos.
5. Tinción Giemsa
5.1. procedimiento
5.1.1. 1.Preparar y fijar el frotis. 2.Aplicar la solución de Giemsa diluida y dejar actuar durante el tiempo recomendado. 3.Lavar, secar y observar al microscopio.
5.1.1.1. Identifica
5.1.1.1.1. parásitos en muestras de sangre y estudio de células sanguíneas.
