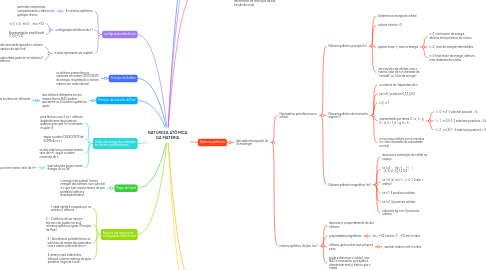
1. configuração eletrônicas
1.1. 4 números quânticos
1.1.1. permitem caracterizar completamente o elétron em qualquer átomo
1.2. configuração eletrônica do H
1.2.1. n=1, l=0 , ml=0 , ms=+1/2
1.2.2. Representação simplificada (1,0,0,+1/2)
1.3. a caixa representa um orgbital
1.3.1. cada semisseta repsenta o número quantico de spin (ms)
1.3.2. cada orbital pode ter no máximo 2 elétrons
2. Princípio de Aufbau
2.1. os elétrons preenchem os subníveis em ordem CRESCENTE de energia, respeitando o número máximo em cada subnível
3. Princípio de exclusão de Pauli
3.1. dois elétrons diferentes em um mesmo átomo NÃO podem apresentar os 4 números quânticos iguais
3.1.1. pelo menos ms deve ser diferente (+/-)
4. Ordem de energia dos subníveis em átomos polieletrônicos
4.1. para átomos com 2 ou + elétrons, depende tanto dos números quâticos principal (n) e momento angular (l)
4.2. segue a ordem CRESCENTE da SOMA de n e l
4.3. se dois subníveis possuem mesmo valor de n+l, seguir a ordem crescente de n
4.4. qual subníveis possui menor energia, 4s ou 3d?
4.4.1. 4s, pois tem menor valor de n+l
5. Regra de Hund
5.1. o arranjo mais estável (menor energia) dos elétrons num subnível é o que tiver maios número de spin paralelos (elétrons desemparelhados)
6. Resumo das regras para configurações eletrônicas
6.1. 1-cada orbital é ocupado por no máximo 2 elétrons
6.2. 2 - 2 elétrons de um mesmo átomos não podem ter os 4 números quânticos iguais (Princípio de Pauli)
6.3. 3 - Nos átomos polieletrônicos os subníveis de nergia são ordenados com a ordem crescente de n+l
6.4. 4-arranjo mais estável dos elétrons: número máximo de spins paralelos (regra de hund)
7. DUALIDADE ONDA-PARTÍCULA (BROGLIE)
7.1. elétron livre de massa m, que se move com velocidade v, tem um comprimeto de onda associado
8. Princípio da incerteza de Heisenberg
8.1. É impossível determinar a posição e a velocidade de um elétron simultaneamente
8.2. O elétron não se move em volta do núcleo com uma trajetória bem definida
9. Orbitais atômicos Schrodinger
9.1. funções de onda de elétrons nos átomos, cujos quadrados determinam a probabilidade de encontrar o elétron ao redor do núcleo
9.2. orbitais atômicos podem ser descritos por 3 números quânticos, decorrentes da resolução da sua função de onda
10. Números quânticos
10.1. derivados da equação de Schrodinger
10.1.1. Necessários para descrever o orbital:
10.1.1.1. Número quântico principal (n)
10.1.1.1.1. Determina a energia do orbital
10.1.1.1.2. valores inteiros >0
10.1.1.1.3. quanto maior n, maior a energia
10.1.1.1.4. um conjunto de orbitais com o mesmo valor de n é chamado de "camada" ou "nível de energia"
10.1.1.2. Número quântico de momento angular (l)
10.1.1.2.1. os valores de l dependem de n
10.1.1.2.2. se n=6, l pode ser 0,1,2,3,4,5
10.1.1.2.3. l=0, n-1
10.1.1.2.4. representado por letras: 0 =s, 1 = p, 2 = d, 3 = f, 4 = g, 5 = h
10.1.1.2.5. um ou mais orbitais com o mesmos n e l são chamados de subcamada ou nível
10.1.1.3. Número quântico magnético (ml)
10.1.1.3.1. descreve a orientação do orbital no espaço
10.1.1.3.2. se l=4, ml=-l, ..., +l = -4,-3,-2,-1,0,1,2,3,4
10.1.1.3.3. se l=0 (s), ml=-l,-,l = 0 ( 1 valor = orbital)
10.1.1.3.4. se l=1, 3 possíveis orbitais
10.1.1.3.5. se l=2, 5 possíveis orbitais
10.1.1.3.6. subníveis 6g com 9 possíveis orbitais
10.1.2. número quântico de spin (ms)
10.1.2.1. descreve o comportamento do dos elétrons
10.1.2.2. propriedades magnéticas
10.1.2.2.1. ms : +1/2 horário // -1/2 anti-horário
10.1.2.3. elétrons giram sobre seus próprios eixos
10.1.2.3.1. sentido horário e anti-horário
10.1.2.4. ajuda a descrever o orbital, mas NÃO é necessário pois ajuda a caracterizar mais o elétron que o orbital
11. Forma dos orbitais
11.1. s > esférico
11.2. p = halteres
11.3. d = dois halteres
11.4. f = representação mais complexa
12. Propriedades magnéticas dos átomos
12.1. átomos paramagnéticos
12.1.1. contém elétrons com spins desemparelhados (paralelos)
12.1.2. são atraídos por um imã
12.2. átomos diamagnéticos
12.2.1. contém elétrons com spins emparelhados (opostos)
12.2.2. levemente repelidos por um imã
