1. La materia la podemos encontrar en la naturaleza en forma de sustancias puras y de mezclas.
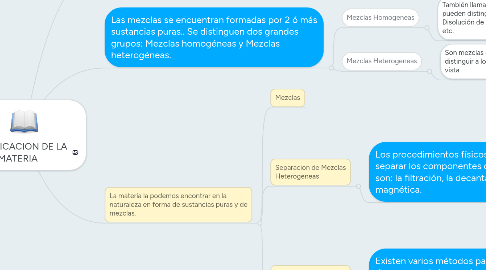
2. Las mezclas se encuentran formadas por 2 ó más sustancias puras.. Se distinguen dos grandes grupos: Mezclas homogéneas y Mezclas heterogéneas.
2.1. Mezclas Homogeneas
2.1.1. También llamadas Disoluciones. Son mezclas en las que no se pueden distinguir sus componentes a simple vista. Ejemplo: Disolución de sal en agua, el aire, una aleación de oro y cobre, etc.
2.2. Mezclas Heterogeneas
2.2.1. Son mezclas en las que se pueden distinguir a los componentes a simple vista
3. La materia la podemos encontrar en la naturaleza en forma de sustancias puras y de mezclas.
3.1. Mezclas
3.2. Separacion de Mezclas Heterogeneas
3.2.1. Los procedimientos físicos más empleados para separar los componentes de una mezcla heterogénea son: la filtración, la decantación y la separación magnética.
3.2.1.1. Filtracion
3.2.1.1.1. Este procedimiento se emplea para separar un líquido de un sólido insoluble.
3.2.1.2. Decantacion
3.2.1.2.1. Esta técnica se emplea para separar 2 líquidos no miscibles entre sí. Ejemplo: Agua y aceite
3.2.1.3. Separacion Magnetica
3.2.1.3.1. Esta técnica sirve para separar sustancias magnéticas de otras que no lo son. Al aproximar a la mezcla el imán, éste atrae a las limaduras de hierro, que se separan así del resto de la mezcla.
3.3. Separacion de Mezclas Homogeneas
3.3.1. Existen varios métodos para separar los componentes de una mezcla homogénea o disolución. Entre los más utilizados están la cristalización y la destilación simple
3.3.1.1. Cristalizacion
3.3.1.1.1. Esta técnica consiste en hacer que cristalice un soluto sólido con objeto de separarlo del disolvente en el que está disuelto.
3.3.1.2. Destilacion simple
3.3.1.2.1. Esta técnica se emplea para separar líquidos de una disolución en función de sus diferentes puntos de ebullición. Es el caso, por ejemplo, de una disolución de dos componentes, uno de los cuáles es volátil
