Kemiske bindinger 3
af jesper andresen
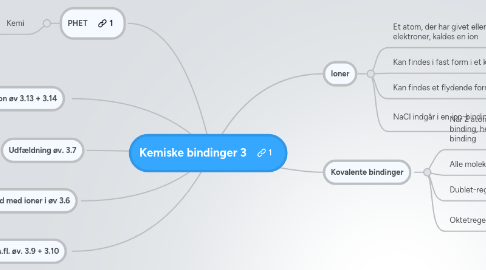

1. Ioner
1.1. Et atom, der har givet eller taget elektroner, kaldes en ion
1.1.1. Ioner kan være positivt eller negativt elektrisk ladet
1.2. Kan findes i fast form i et krystal
1.2.1. Bundet sammen med elektriske kræfter
1.3. Kan findes et flydende form i væske
1.3.1. Ionerne bevæger sig rundt i væsken
1.4. NaCl indgår i en ion-binding i et krystal
2. Kovalente bindinger
2.1. Når 2 atomer deler 2 elektroner i en binding, hedder det en kovalent binding
2.2. Alle molekyler indeholder kovalente bindinger
2.3. Dublet-regel
2.3.1. i H-H opfylder H dubletregelen
2.4. Oktetregel
2.4.1. I H-O-H opfylder O oktetregelen og H dubletregelen
3. Udfældning øv. 3.7
4. Vand med ioner i øv 3.6
4.1. Krystalvand
5. Smørsyre, myresyre m.fl. øv. 3.9 + 3.10
6. En prik = En elektron øv 3.13 + 3.14
7. PHET
7.1. Kemi
7.1.1. Afstemning af kemiske ligninger
7.1.2. Byg et atom
7.1.3. Byg et molekyle
7.1.4. Molekyleformer
