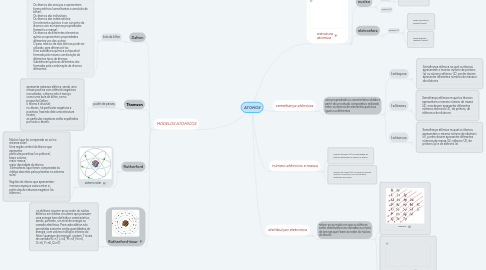
1. MODELOS ATOMICOS
1.1. Dalton
1.1.1. bola de bilhar
1.1.1.1. Os átomos são maciços e apresentam forma esférica (semelhantes a uma bola de bilhar); Os átomos são indivisíveis; Os átomos são indestrutíveis; Um elemento químico é um conjunto de átomos com as mesmas propriedades (tamanho e massa); Os átomos de diferentes elementos químicos apresentam propriedades diferentes uns dos outros; O peso relativo de dois átomos pode ser utilizado para diferenciá-los; Uma substância química composta é formada pela mesma combinação de diferentes tipos de átomos; Substâncias químicas diferentes são formadas pela combinação de átomos diferentes..
1.2. Thomson
1.2.1. pudim de passas
1.2.1.1. apresenta natureza elétrica, sendo uma massa positiva com elétrons negativos incrustados. o átomo não é maciço como uma bola de bilhar, como propunha Dalton; o átomo é divisível; no átomo, há partículas negativas e positivas, fazendo dele uma estrutura neutra; as partículas negativas estão espalhadas por todo o átomo.
1.3. Rutherford
1.3.1. sistema solar
1.3.1.1. Núcleo (que foi comparado ao sol no sistema solar) Uma região central do átomo que apresenta: partículas positivas (os prótons); baixo volume; maior massa; maior densidade do átomo. Eletrosferas (que foram comparadas às órbitas descritas pelos planetas no sistema solar) Regiões do átomo que apresentam: imensos espaços vazios entre si; partículas de natureza negativa (os elétrons).
1.4. Rutherford-bour
1.4.1. ,os elétrons movem-se ao redor do núcleo atômico em órbitas circulares que possuem uma energia bem definida e característica, sendo, portanto, um nível de energia ou camada eletrônica. Para cada elétron são permitidas somente certas quantidades de energia, com valores múltiplos inteiros do fóton (quantum de energia). contem 7 niveis de camada (K=n1, L=n2, M=n3, N=n4, O=n5, P=n6, Q=n7).
2. estrutura atomica
2.1. nucleo
2.1.1. Neutrons
2.1.1.1. nao paresentam carga
2.1.2. Protons (+)
2.2. eletrosfera
2.2.1. Eletrons (-)
2.2.1.1. perda de eletrons: positivo (ânios)
2.2.1.2. ganha eletrons: negativo (cátion)
3. número atômicos e massa
3.1. Número atômico (Z): é a quantidade de prótons existentes no núcleo do átomo
3.2. Número de massa (A): e a soma do número atômico ou prótons, com os nêutrons existentes no núcleo.
4. semelhança atômicas
4.1. uma propriedade ou característica obtida a partir de um estudo comparativo realizado entre os átomos de elementos químicos iguais ou diferentes
4.1.1. Isótopos
4.1.1.1. Semelhança atômica na qual os átomos apresentam o mesmo número de prótons (p) ou número atômico (Z), porém devem apresentar diferentes números de massa e de nêutrons
4.1.2. Isóbaros
4.1.2.1. Semelhança atômica na qual os átomos apresentam o mesmo número de massa (A), mas devem apresentar diferentes números atômicos (Z), de prótons, de elétrons e de nêutrons
4.1.3. Isótonos
4.1.3.1. Semelhança atômica na qual os átomos apresentam o mesmo número de nêutrons (n), porém devem apresentar diferentes números de massa (A), atômico (Z), de prótons (p) e de elétrons (e).
5. distribuiçao eletronica
5.1. refere-se ao modo em que os elétrons estão distribuídos nas camadas ou níveis de energia que ficam ao redor do núcleo do átomo
5.1.1. diagrama
5.1.2. tabela de niveis
