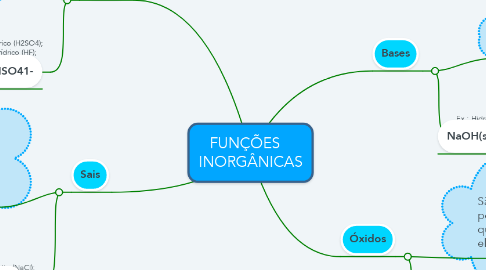
FUNÇÕES INORGÂNICAS
by Leticya Oliveira
1. Ácidos
1.1. Formam hidrônio (H3O+) na reação com a água.
1.2. Ex.: Ácido Sulfúrico (H2SO4); Ácido Fluorídrico (HF); Ácido Clorídrico (HCl).
2. Sais
2.1. São compostos capazes de se dissociar na água, liberando íons, mesmo em pequena porcentagem, dos quais pelo menos um cátion é diferente de H3O1+ e pelo menos um ânion é diferente de OH1-.
2.2. Ex.: Cloreto de Sódio (NaCl); Fluoreto de sódio (NaF).
3. H2SO4 → H3O1+ + HSO41-
4. NaCl → Na1+ + Cl1-
5. Bases
5.1. Sofrem dissociação em água e liberam hidroxila (OH-).
5.2. Ex.: Hidróxido de sódio (NaOH); Hidróxido de cálcio (Ca(OH)2).
6. Óxidos
6.1. São compostos binários (formados por apenas dois elementos químicos), e o oxigênio é o elemento mais eletronegativo.
6.2. Ex.: CO2 (Dióxido de carbono); SO2 (Dióxido de enxofre).
7. NaOH(s) → Na1+ + OH1-


